








Категория: Бланки/Образцы
АЛГОРИТМ ДЕЙСТВИЯ СОТРУДНИКА АПТЕЧНОГО УЧРЕЖДЕНИЯ, ВЫЯВИВШЕГО ФАЛЬСИФИЦИРОВАННОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО
"Аптечный бизнес", 2009, N 7
Анализ практики деятельности участников фармрынка по изъятию из обращения и уничтожению фальсифицированных и недоброкачественных лекарственных препаратов свидетельствует о том, что эта работа фактически не ведется, и не только потому, что участники фармрынка не желают изымать из оборота и уничтожать эти лекарства, но и потому, что отсутствуют соответствующие рекомендации и контроль за этим процессом.
В целях единообразия действий по борьбе с распространением фальсифицированных лекарств, на обсуждение сотрудников аптечных учреждений предлагается проект Инструкции "О действиях сотрудников аптечных учреждений при обнаружении фальсифицированных лекарственных средств".
1. Руководители и владельцы аптечных учреждений обязаны организовать работу по своевременному получению, хранению и дальнейшему использованию информации Росздравнадзора о фальсифицированных и недоброкачественных лекарственных препаратах, с целью своевременного обнаружения таких лекарств среди хранящихся - закупленных ранее, а также во избежание закупки таких ЛС. При этом следует руководствоваться характеристиками фальсифицированных лекарственных средств, изложенными в информации (письмах) Росздравнадзора: фальсифицированной может быть вся серия, либо фальсификат может отличаться от оригинального препарата отличительными признаками, большинство из которых возможно установить визуально при осмотре лекарства и его упаковки.
2. Сотрудник аптечного учреждения, ответственный за качество ЛС, обязан сравнить лекарственное средство и его упаковку с указанными в письме Росздравнадзора отличительными признаками фальсификации и при их обнаружении обязан приостановить дальнейший оборот этого фальсифицированного лекарства, изъяв его из оборота.
2.1. Если не один из отличительных признаков, указанных в письме Росздравнадзора, не обнаружен на ЛС, имеющемся в аптечном учреждении, то это ЛС не является фальсифицированным, поэтому подлежит дальнейшему обороту. По факту проверки составляется справка в двух экземплярах: первый приобщается к накладной, второй направляется в территориальное управление Росздравнадзора в качестве информации.
2.2. В том случае, если в аптечном учреждении имеются аналогичные ЛС, но с другими сериями, которые не указаны в информации Росздравнадзора как фальсифицированные, то и их необходимо проверить по отличительным признакам на предмет фальсификации. При наличии на таких ЛС признаков фальсификации их оборот необходимо приостановить, поместить в карантинную зону с актом "о выявлении лекарственных средств, вызвавших сомнение в подлинности", и сообщить в территориальное управление Росздравнадзора для проведения мероприятий по проверке качества ЛС, направив туда копию акта и две упаковки с ЛС в качестве образца для исследования.
2.3. Если аптечное учреждение, получив информацию Росздравнадзора о фальсифицированных лекарствах, установит, что такие ЛС ранее в течение года были закуплены, но уже проданы, то информацию в форме сообщения о таких лекарствах и поставщике необходимо направить в территориальное управление Росздравнадзора и органы внутренних дел (далее - ОВД).
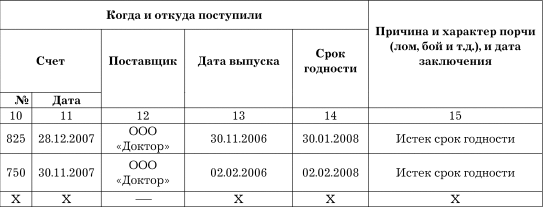
3. Факт изъятия из оборота фальсифицированных лекарственных средств, указанных в п. 2. и 2.2. оформляется комиссией в составе не менее трех человек путем составления акта об обнаружении фальсифицированных лекарств (либо вызвавших сомнение в подлинности) в четырех экземплярах (первый остается с ЛС в карантинной зане; второй направляется в территориальное управление Росздравнадзора; третий вместе с материалом направляется в ОВД; четвертый вместе с накладной передается в бухгалтерию). После чего это лекарство с копией акта помещается в карантинную зону, изолированно от всех лекарств и других товаров. В акте об обнаружении фальсифицированных лекарственных средств либо в акте о выявлении лекарственных средств, вызвавших сомнение в подлинности, кроме прочего, должно быть указано:
название лекарственного препарата, его серия, лекарственная форма, дозировка, срок годности и производитель;
номер и дата письма Росздравнадзора, в котором данное ЛС признано фальсифицированным и указано на необходимость его изъятия из обращения либо о приостановлении;
наличие признаков, по которым, согласно письму Росздравнадзора, это фальсифицированное лекарство отличается от оригинального ЛС (либо отметить факт фальсификации всей серии);
отличительные признаки, которые обнаружены у конкретного ЛС;
номер и дата накладной, по которой было получено данное ЛС;
название организации, у которой было получено данное ЛС;
количество полученных упаковок ЛС, указанное в накладной;
количество упаковок ЛС, оставшихся в наличии на день установления его фальсифицированности (вызвавшим сомнение в подлинности);
количество упаковок фальсифицированных лекарственных средств, направленных в ОВД в качестве образца (направляется две упаковки). В акте также отражается, что направляемые образцы фальсифицированных лекарственных средств упакованы в полиэтиленовый пакет, который перевязан шпагатом (прочной ниткой), концы которого оклеены листком бумаги небольшого формата с нанесенным на нем оттиском печати организации, датой и подписью лиц (не менее трех), упаковавших его и составивших акт;
фактическое количество упаковок обнаруженных фальсифицированных лекарственных средств, находящихся с актом в карантинной зоне.
4. Руководитель либо владелец аптечного учреждения в письменной форме сообщает в территориальное подразделение органа внутренних дел об обнаружении фальсифицированных лекарственных средств и передает заявление с соответствующими материалами и образцами фальсифицированных лекарственных средств сотруднику ОВД. Сотрудник ОВД должен принять указанное заявление, материал, образцы этих лекарств, подтвердив факт их приемки личной подписью на копии заявления. При отсутствии возможности непосредственной передачи сотруднику органов внутренних дел указанных заявления, материалов, образцов руководитель, владелец аптечного учреждения либо уполномоченное ими лицо принимает необходимые меры по направлению заявления, материалов, образцов в органы внутренних дел в день обнаружения фальсифицированных лекарственных средств. К заявлению прилагаются следующие документы или их заверенные аптечным учреждением копии:
копия товарной накладной;
копия декларации о соответствии ЛС;
копия лицензии, полученной от поставщика данного ЛС;
копия лицензии аптечного учреждения на осуществление фармацевтической деятельности с приложением;
копия акта об обнаружении и изъятии ФЛС из оборота и размещении их в карантинной зоне;
копия письма Росздравнадзора, которым эти ЛС признаны фальсифицированными.
В заявлении необходимо указать весь перечень направляемых документов, название и количество лекарственных средств, направляемых в качестве образца.
5. Сотрудники ОВД, приступив к проверке заявления, обязаны изъять фальсифицированное лекарство из аптечного учреждения и хранить в порядке, установленном для хранения вещественных доказательств, либо оставить в аптечном учреждении на ответственное хранение. Фальсифицированное лекарственное средство может быть уничтожено только по решению суда. При возбуждении уголовного дела по результатам проверки материалов об обращении фальсифицированных лекарственных средств, заявитель, которому причинен ущерб в результате приобретения таких ЛС, признается потерпевшим, которому по решению суда возмещается причиненный ущерб.
6. О направлении материала в ОВД по факту выявления фальсифицированных лекарственных средств руководитель либо владелец аптечного учреждения сообщает в территориальное управление Росздравнадзора, направляя туда копию акта о выявленном фальсифицированном лекарстве.
Следует отметить, что к продукции, не соответствующей требованиям технического регламента, т.е. к некачественной, Росздравнадзор относит забракованные лекарственные средства, которые, после того как Росздравнадзор признает их таковыми, можно возвращать поставщику.
Забракованные лекарственные средства нельзя путать с недоброкачественными лекарственными средствами, так как это не одно и то же. В законе о лекарственных средствах недоброкачественным лекарственным средствам дано следующее определение: это лекарственное средство, пришедшее в негодность, и (или) лекарственное средство с истекшим сроком годности.
При выявлении недоброкачественных лекарственных средств владелец обязан изъять их из обращения, составить акт, поместить в карантинную зону, а затем уничтожить в соответствии с Инструкцией. Сообщать о таких лекарственных средствах в органы внутренних дел нет необходимости. За торговлю заведомо некачественными ЛС, т.е. забракованными, недоброкачественными и фальсифицированными лекарственными средствами наступает административная либо уголовная ответственность.
Выполнение указанных рекомендаций повысит исполнительскую дисциплину участников фармрынка и избавит их от административной и уголовной ответственности.
Старший научный сотрудник
ВНИИ МВД России

Современные автоматизированные системы (1С Аптека и т.д.), которые используют в аптечных организациях облегчают контроль за забракованными сериями лекарственных препаратов.
Управление движением лекарственными препаратами основано на учете серий товара на всем пути его продвижения - от производства до реализации конечному потребителю. Система контроля подлинности и качества лекарств, реализуемых на территории России, также оперирует понятием серии лекарственного препарата. Так как лекарства из одной серии должны иметь однородные показатели по всем параметрам, их анализ основывается на выборке из серии, в результате анализа которой принимается решение о допуске всей серии к реализации.
Основой для признания серии лекарственных препаратов фальсифицированной или забракованной служит письмо Росздравнадзора. Эти письма в полном объеме публикуются на официальном портале учреждения - www.roszdravnadzor.ru. а также дублируются на нескольких других сайтах.
Аптека может получить эти информационные материалы несколькими способами:
- самостоятельно - используя информацию в Интернете (сайт Росздравнадзора);
- использует письма от своих поставщиков (некоторые дистрибьюторы предоставляют аптеке распечатки писем Росздравнадзора о фальсифицированных/забракованных лекарственных препаратах в качестве дополнительного сервиса);
- отслеживают списки фальсифицированных/забракованных серий препаратов из офиса своей аптечной сети в электронном или бумажном виде (менеджеры аптечной сети).
При получении новой информации о фальсификатах аптечная организация организует проверку лекарственных препаратов и устанавливает, есть ли такие лекарства среди товарных запасов аптеки.
Алгоритм действий аптеки, в случае выявления фальсифицированного лекарственного препарата:
1. Заведующие и директора аптечных организаций должны организовать работу по своевременному получению, хранению и дальнейшему использованию информации Росздравнадзора о фальсифицированных и недоброкачественных лекарственных препаратах с целью своевременного обнаружения таких лекарств (информационные письма Росздравнадзора).
2. Персонал аптеки обязан сравнить лекарственный препарат, его упаковку и маркировку с указанными в письме отличительными признаками и, обнаружив их, обязан приостановить дальнейший оборот этого фальсифицированного лекарственного препарата, изъяв его из оборота.
3. Факт изъятия из оборота лекарственного препарата, обладающего признаками фальсификации, оформляется составлением акта об обнаружении фальсифицированного лекарственного препарата. Затем фальсифицированный лекарственных препарат с копией акта помещается в особую карантинную зону.
Интересные статьи:Постановлением Правительства Российской Федерации от 30.06.2004 № 323 «Об утверждении Положения о Федеральной службе по надзору в сфере здравоохранения» (п.5.1.4.2.) на Росздравнадзор возложены полномочия по федеральному государственному надзору в сфере обращения лекарственных средств посредством проведения проверок соответствия лекарственных средств установленным обязательным требованиях к их качеству.
В разделе «Нормативные документы» размещены: нормативные акты, которые определяют требования к лекарственным средствам на этапах их обращения (контроль качества на стадии производства, хранения, реализации); информационные письма Росздравнадзора, где указываются лекарственные средства, подлежащие изъятию; информационно-аналитические материалы о результатах проверок Росздравнадзора.
Информационные письмаОб отзыве из обращения лекарственного препарата
О соответствии лекарственных средств требованиям нормативной документаци
О соответствии лекарственных средств требованиям нормативной документаци
О прекращении обращения серии лекарственного средства
О снятии лекарственного средства с несерийного выборочного контроля качества и переводе на выборочный контроль качества
Ответы на часто задаваемые вопросыОпределить соответствие установленным обязательным требованиям к качеству лекарственных препаратов возможно на базе испытательных лабораторий, имеющих в области аккредитации указание о возможности проведения экспертизы лекарственных средств.
Предпочтительным форматом направления данной информации является «Извещение о побочном действии, нежелательной реакции или отсутствии ожидаемого терапевтического эффекта лекарственного средства», которое доступно для загрузки с интернет-сайта Росздравнадзора .
Лекарственное средство является особым товаром, к приобретению которого гражданам следует относиться очень ответственно. При покупке препарата потребитель вправе ознакомиться с товаром, запросить дополнительные сведения о нем, в том числе информацию о подтверждении соответствия его качества.
Отдел организации контроля качества лекарственных средств
Тарасова Светлана Анатольевна

Справочная Росздравнадзора: +7 (495) 698-45-38, +7 (499) 578-02-30
Адрес: 109074, Москва, Славянская площадь, д. 4, стр. 1
Содержит информацию по фальсифицированным и запрещенным к продаже медицинским препаратам, нормативным документам по контролю качества лекарственных средств, фальсификатам, обнаруженным в розничной сети. Обновление информации в программе обычно происходит 3-4 раза в день. Дата обновления - 22.12.2016 в 18:00

 Заказ товара поставщику. Подготовка и обработка заказов поставщику.
Заказ товара поставщику. Подготовка и обработка заказов поставщику.
 Настройки прав доступа для сотрудников аптеки.
Настройки прав доступа для сотрудников аптеки.
 Оформление нового протокола согласования цен для розницы.
Оформление нового протокола согласования цен для розницы.
 Оформление возврата поставщику товара из аптеки.
Оформление возврата поставщику товара из аптеки.
 Скидки при реализации лекарств. Настройка скидки с подтверждением при продаже. Настройка скидок по времени.
Скидки при реализации лекарств. Настройка скидки с подтверждением при продаже. Настройка скидок по времени.
 Печать этикеток со штрих-кодом на обычный принтер и принтер штрих-кодов. Печать штрих-кодов по количеству товара.
Печать этикеток со штрих-кодом на обычный принтер и принтер штрих-кодов. Печать штрих-кодов по количеству товара.
 Обзор новых нормативных документов в области здравоохранения, вступивших в силу с января 2016 года.
Горячая линия
Обзор новых нормативных документов в области здравоохранения, вступивших в силу с января 2016 года.
Горячая линия

для приема обращений по вопросам качества лекарственных средств:
8-800-775-36-03

База данных забракованных медицинских средств. Перечень обновляется ежедневно, содержит ссылки на нормативные документы, согласно которым препарат признан фальсификатом. В настоящий момент в базе около 25 000 лекарственных препаратов.
Нормативные документы.
Тексты нормативных документов, регулирующие фармацевтическую, медицинскую деятельность и контроль качества лекарственных средств. Новые документы подключаются 3-4 раза в неделю. В настоящий момент в базе более 16 000 нормативных документов.
ЦЕНТР КОНТРОЛЯ КАЧЕСТВА
Воронежский центр контроля качества и сертификации лекарственных средств был создан для предотвращения оборота фальсифицированных и недоброкачественных лекарственных средств. Центр непосредственно работает под руководством Департамента здравоохранения Воронежской области и в тесном взаимодействии с Федеральным и территориальным управлением Росздравнадзора, Роспотребнадзора, Прокуратурой и правоохранительными органами Воронежской области. В составе Центра функционируют отдел контроля качества (испытательная лаборатория), отдел фармацевтической информации и отдел сертификации и инспекционного контроля.
Фармацевтика и медицина. Статьи и публикации.
В этом разделе можно ознакомиться с информацией по следующей тематике: Производители фармацевтической продукции. Фальсификаты. Подделка лекарственных препаратов.
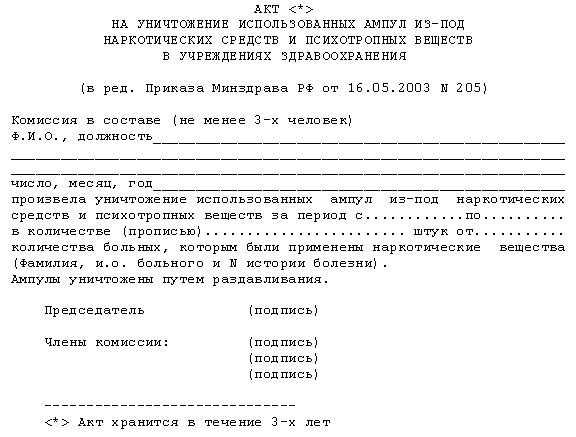
В соответствии с пунктом 2 утвержденных Постановлением Правительства РФ от 03.09.2010 №674 "Правил уничтожения недоброкачественных лекарственных средств, фальсифицированных лекарственных средств и контрафактных лекарственных средств" (в ред. от 16.01.2016) недоброкачественные лекарственные средства подлежат изъятию и уничтожению по решению владельца указанных лекарственных средств, решению Федеральной службы по надзору в сфере здравоохранения или решению суда.



"Недоброкачественное лекарственное средство" - лекарственное средство, не соответствующее требованиям фармакопейной статьи либо в случае ее отсутствия требованиям нормативной документации или нормативного документа (пункт 38 статьи 4 Федерального закона РФ № 61 "Об обращении лекарственных средств").
Согласно пункту 10 указанных Правил владелец недоброкачественных лекарственных средств, принявший решение об их изъятии, уничтожении и вывозе, передает указанные лекарственные средства организации, осуществляющей уничтожение лекарственных средств, на основании соответствующего договора.
В соответствии с пунктами 11-13 Правил организация, осуществляющая уничтожение лекарственных средств, составляет акт об уничтожении лекарственных средств, в день уничтожения лекарственных средств. Акт об уничтожении лекарственных средств или его копия, заверенная в установленном порядке, в течение 5 рабочих дней со дня его составления направляется владельцем уничтоженных лекарственных средств в Федеральную службу по надзору в сфере здравоохранения.


При выявлении лекарственных средств с истекшим сроком годности они должны храниться отдельно от других групп лекарственных средств в специально выделенной и обозначенной (карантинной) зоне (пункт 12 утвержденных Приказом Минздравсоцразвития РФ №706н "Правил хранения лекарственных средств" )
Больше никаких упоминаний об организации работы в аптечной организации с недоброкачественными лекарственными средствами, а также об организации в аптеке так называемой карантинной зоны действующее законодательство в сфере обращения лекарственных средств не содержит. Единственные установленные законодательством требования к карантинной зоне - это специально выделенная и обозначенная .
Согласно Общей фармакопейной статье "Хранение лекарственных средств" ОФС.1.1.0010.15 забракованные лекарственные средства должны быть идентифицированы и храниться в соответствующем помещении (зоне) в условиях, не допускающих их несанкционированного использования .
С учетом данного обстоятельства руководитель аптечной организации вправе самостоятельно определить порядок действий по размещению и хранению недоброкачественных лекарственных средств до их передачи для последующего уничтожения, а также порядок размещения и оснащения карантинной зоны для хранения таких лекарственных средств.
Другие интересные статьи:Если покупатель возвращает тонометр в аптеку
Запись навигация